為了進一步規(guī)范允許保健食品聲稱的保健功能目錄的管理工作,國家市場監(jiān)督管理總局發(fā)布并實施了《保健食品原料目錄與保健功能目錄管理辦法》和《保健食品新功能及產(chǎn)品技術(shù)評價實施細則(試行)》,正式開放保健食品新功能的申報,推動保健食品新功能創(chuàng)新。
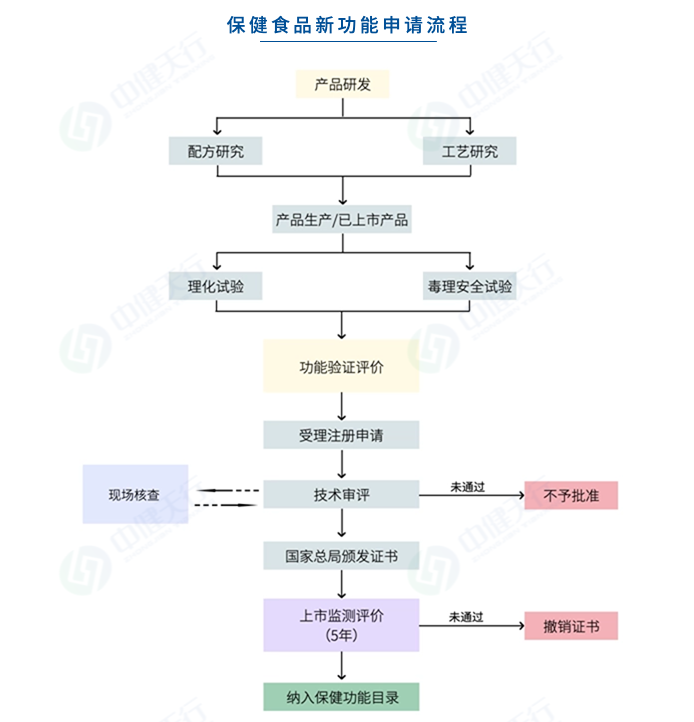
保健食品新功能的申報材料要求
建議人提交新功能建議時,應(yīng)當(dāng)按照《實施細則》附表“保健食品新功能建議材料項目要求和技術(shù)評價要點”提供技術(shù)評價材料,具體材料項目為:
1. 新功能建議材料目錄
2. 建議人對提交材料真實性負責(zé)的承諾書
3. 建議人身份證明或主體登記證明文件復(fù)印件
4. 保健功能名稱、解釋、機理及其依據(jù)
5. 保健功能研究報告
6. 保健功能評價方法及驗證評價資料
7. 相同或者類似保健功能在國內(nèi)外的應(yīng)用情況
8. 有助于技術(shù)評價的科學(xué)文獻依據(jù)及其他相關(guān)材料
9. 保健功能倫理學(xué)相關(guān)材料
10. 新功能研究樣品技術(shù)評價相關(guān)材料
11. 其他與功能建議和評價相關(guān)的材料
12. 其他人群試食試驗評價相關(guān)資料
13. 其他需要說明的問題
自2019年《保健食品原料目錄與保健功能目錄管理辦法》發(fā)布,就已有很多企業(yè)提前布局,在進行保健食品新功能的開發(fā),近幾年我們已陸續(xù)幫助完成幾款新功能產(chǎn)品的動物模型篩選以及人體試驗評價,獲得寶貴的新功能開發(fā)經(jīng)驗,歡迎新功能申報企業(yè)來電與我們交流,我們會為您介紹新功能新產(chǎn)品研發(fā)新方向,并對申報的新功能產(chǎn)品進行全面評估及分析,提供經(jīng)濟、可行、保障的申報方案。